Gynäkologie - Bösartige Erkrankungen - Brust
Die histopathologische Beurteilung von Brustbiopsien erfolgt in 5 Kategorien der sogenannten B-Klassifikation, die von der National Coordinating Group for Breast Screening Pathology (NHSBSP) und der E. C. Working Group on Breast Screening Pathology empfohlen wird. Diese Klassifikation dient der international einheitlichen Kommunikation zwischen Pathologen, Radiologen und Gynäkologen und wird ergänzend zur histologischen Diagnose angegeben. Demnach werden unter der Kategorie B3 vielfältige histopathologische Entitäten zusammengefasst, die als gutartig, aber mit unsicherem biologischen Potenzial eingestuft werden. Zur Kategorie B2, die keine Karzinomwahrscheinlichkeit aufweisen, gehören das Fibroadenom, das Hamartom und die gewöhnliche duktale Hyperplasie (UDH, "u" für usual).
Die Veränderungen der Kategorie B3 können auf das synchrone Vorliegen einer höhergradigen Veränderung in der Brust hinweisen (Indikatorläsion) oder das Risiko für die Entstehung von Brustkrebs erhöhen (Vorläuferläsion). B3-Läsionen werden häufig im Rahmen einer Stanz- oder Vakuumbiopsie als Zufallsbefund entdeckt, wobei sie aufgrund ihrer Assoziation mit Mikrokalk seit Einführung des Mammografie-Screenings zunehmend entdeckt werden.
Das therapeutische Vorgehen bei Nachweis solcher Veränderungen wird aufgrund ihres variablen Progressionsrisikos kontrovers diskutiert. Trotz ihres unklaren biologischen Verhaltens gelten B3-Läsionen als gutartige Veränderungen, bei deren Detektion die Herausforderung darin besteht, abzuwägen, in welchen Fällen einer operative Exzision durchgeführt werden sollte, um z. B. ein assoziiertes Krebsleiden nicht zu übersehen, jedoch zeitgleich keine Übertherapie zu betreiben.
Zu den B3-Läsionen mit geringem Malignitätsrisiko zählen Papillome ohne Atypie, radiäre Narben, gutartige Phylloidestumoren und die flache epitheliale Atypie. Mit zunehmenden Risiken für die Entwicklung einer bösartigen Entwicklung nach Exzisionsbiopsien ist hingegen bei atypischen Papillomen, der atypischen duktalen Hyperplasie und der lobulären intraepithelialen Neoplasie zu rechnen.
Flache epitheliale Atypie (FEA):
Eine FEA entsteht durch den Ersatz des nativen Epithels durch eine Schicht von gering bis mittelgradig atypischen Zellen. Es besteht eine Assoziation mit Zysten und häufig liegen Mikrokalzifikationen vor. Die klinische Relevanz einer FEA wird kontrovers diskutiert. Einerseits werden in der Nachbarschaft einer FEA oftmals koexistente höhergradige Veränderungen (z. B. ADH, lobuläre Neoplasie, low-grade DCIS und gut differenzierte invasive Karzinome) gefunden, so dass eine FEA als Indikatorläsion angesehen werden kann. Andererseits bestehen aufgrund zytologischer, immunhistochemischer und molekulargenetischer Ähnlichkeiten auch Hinweise darauf, eine FEA als mögliche Vorläuferläsion solcher Veränderungen annehmen zu können. Das Risiko der Entwicklung eines bösartigen Tumors wird als sehr gering angegeben. Nach der Diagnose einer FEA wird eine Mammographie alle 2 Jahre empfohlen.
Atypische duktale Hyperplasie (ADH):
Zur Gruppe der intraduktalen proliferativen Läsionen gehört auch die atypische duktale Hyperplasie, die charakterisiert ist durch eine Proliferation gleichförmiger homogen verteilter Zellen, die architektonisch und zytologisch den Zellen eines low-grade duktalen Carcinoma in situ (DCIS) entsprechen. Die Differenzierung zwischen ADH und low-grade DCIS erfolgt im Wesentlichen durch quantitative Kriterien. Danach ist in der Regel eine ADH nicht größer als 2 mm. Die ADH gilt als potenzielle Vorläuferläsion. Das Risiko für die Entstehung eines späteren Mammakarzinoms ist um das 3- bis 5-Fache erhöht und betrifft beide Brüste. Die Nachsorge besteht aus einer jährlichen Mammographie.
Intraduktale Papillome:
Das solitäre Papillom entsteht in einem Hauptmilchgang, ist üblicherweise hinter der Brustwarze gelegen und wird synonym daher auch als zentrales Papillom bezeichnet. Periphere Papillome, welche seltener sind, nehmen ihren Ursprung typischerweise peripher im Brustgewebe und treten meist an mehreren Stellen auf, weshalb sie in diesen Fällen auch multiple Papillome genannt werden. Häufig finden sich innerhalb eines Papilloms auch Herde intraduktaler Epithelproliferationen. Handelt es sich dabei nicht nur um eine einfache Epithelhyperplasie (UDH), sondern um atypische Proliferationen, die einer ADH oder einem kleinen low-grade DCIS gleichen, spricht man von einem atypischen Papillom. Diese Veränderungen sind häufiger mit peripheren Papillomen assoziiert, können aber auch Teil eines solitären Papilloms sein. Zahlreiche Studien haben ein erhöhtes Brustkrebsrisiko bei Patientinnen mit intraduktalen Papillomen mit und ohne Atypien belegt, wobei dieses Risiko bei atypischen Papillomen deutlich überwiegt. Die operative Exzision eines Papilloms mit Atypie gilt daher als das zu empfehlende Standardverfahren. Die Assoziation dieser Läsionen mit simultanen in situ oder invasiven Karzinomen wird mit bis zu 20 % angegeben, das 5-Jahres-Risiko für die Entstehung eines Karzinoms mit bis zu 13 %. Für das therapeutische Vorgehen bei einem solitären Papillom ohne Atypie gibt es noch keine eindeutige Empfehlung. Mammographische Kontrollen sollten bei Papillomen ohne Atypien alle 2 Jahre, mit Atypien jährlich erfolgen.
Lobuläre intraepitheliale Neoplasie (LIN):
Unter dem Begriff der LIN werden die folgenden beiden Läsionen verstanden: die atypisch lobuläre Hyperplasie (ALH) und das lobuläre Carcinoma in situ (LCIS). Beide Läsionen repräsentieren ein morphologisches Kontinuum, deren Unterscheidung (analog der Differenzierung zwischen ADH und DCIS) durch quantitative Kriterien erfolgt, d. h. abhängig von Ausdehnung und Ausmaß der atypischen Epithelproliferation. Die Bedeutsamkeit einer LIN liegt in ihrem gehäuften multizentrischen (46-85 %) und beidseitigen Vorkommen (30-67 %), das erhöhte Karzinomrisiko gilt dementsprechend sowohl für beide Brüste. Die operative Exzision einer LIN wird empfohlen. Als Ausnahme von der operativen Exzision kann die ALH verbleiben, wenn sie als Zufallsbefund im Randbereich einer anderen bildgebenden Veränderung auftritt und selbst kein radiologisches Korrelat aufweist. Frauen, bei denen eine LIN diagnostiziert wurde, haben ein 7-fach erhöhtes Risiko für das Auftreten eines gleich- oder gegenseitigen Brustkrebses in den nächsten 10 Jahren. Sie sollten eine Mammographie alle 12 Monate erhalten.
Komplexe sklerosierende Läsion:
Der Begriff der radiären Narbe bezieht sich auf kleine Läsionen, die selten größer als 1 cm sind. Die komplex sklerosierende Läsion hingegen verweist auf Befunde, die zwar sämtliche Merkmale der radiären Narbe aufweisen, aber in ihrer Struktur noch heterogener aufgebaut sind und typischerweise >1 cm messen. In der Nachbarschaft mammographisch detektierter radiär sklerosierender Läsionen sind insbesondere bei einer Größe >0,6 cm und bei Frauen >50 Jahre des Öfteren höhergradige Befunde wie ADH, DCIS und invasive Karzinome nachweisbar. In der Regel gilt der Nachweis einer radiären Narbe oder komplex sklerosierenden Läsion in Stanz- oder Vakuumbiopsie als Indikation für eine operative Exzision. Die Nachsorge erfolgt bei alleiniger radiär sklerosierender Läsion durch Mammographie alle 2 Jahre.
Phylloidestumor (PT):
Phylloidestumoren werden in gutartig, borderline und bösartig unterteilt, wobei gutartige PT mit bis zu 75 % überwiegen. PT präsentieren sich meist als schnell wachsende, pralle, mobile Tastbefunde und sind bei einer mittleren Größe von 5 cm in der Regel bei der klinischen Untersuchung nachweisbar. So wird unabhängig vom Differenzierungsgrad standardmäßig die operative Exstirpation mit ausreichendem Sicherheitsrand (≥5 mm) als adäquates Management angesehen, je nach Tumor- bzw. Brustgröße mitunter auch eine Brustamputation. Mit Lokalrezidiven nach brusterhaltender Therapie ist in durchschnittlich 21 % der Fälle zu rechnen. Das Risiko für Fernmetastasen liegt bei malignen PT bei unter 10 %.
Diagnostik:
Für Patientinnen mit Brustkrebs, unklaren oder verdächtigen Befunden sowie Krebsvorstufen stehen neben der sorgfältigen klinischen Untersuchung folgende Untersuchungen zur Verfügung:
- die kurative Mammographie inklusive mammographischer Zusatzaufnahmen wie zum Beispiel der Vergrößerungsmammographie (die kurative Mammographie beschreibt somit eine Mammographie, die außerhalb des Screenings zur Abklärung von Befunden oder Beschwerden durchgeführt wird)
- die Mammasonographie (Brustultraschall) mit Hochfrequenzsonden (7,5–12 MHz analog der Empfehlung der Deutschen Gesellschaft für Ultraschall in der Medizin, DEGUM)
- die interventionellen Methoden wie Stanzbiopsie und Vakuumbiopsie
- in besonderen Fällen die MRT mit Kontrastmittelgabe und die Galaktographie
Diese nichtinvasiven und invasiven diagnostischen Methoden ermöglichen in Kombination mit der histologischen Aufarbeitung der präoperativ entnommenen Stanzen inklusive der dort gewonnenen immunhistochemischen Befunde, nämlich Östrogen- und Progesteronrezeptor (ER/PR), HER2/neu-Status (HER2, „human epidermal growth factor receptor 2“), Grading und Antigen Ki-67, im Rahmen eines prätherapeutischen Konsils eine gezielte Operationsplanung gegebenenfalls unter Berücksichtigung einer neoadjuvanten Systemtherapie. HER2/neu ist ein sogenannter Wachstumsfaktorrezeptor, welcher eine Zellproliferation stimuliert. Eine Überexpression dieses Rezeptors im Tumor ist mit einem schnelleren Tumorwachstum und einer schnelleren Tumorausbreitung verbunden. Das Antigen Ki-67 ist ein Proliferationsmarker, d.h. er färbt die Zellen im Gewebe an, die sich vermehren, die so genannte Wachstumfraktion. Günstig ist ein niedriger Wert bis ca. 10%. Werte zwischen 10 und 30% gelten als intermediäre Werte, Werte darüber als hoch.
| Subtyp | Häufigkeit | ER | PR | HER2/neu | Ki-67/MIB-1 | Grading | Prognose |
|---|---|---|---|---|---|---|---|
| Luminal A |
25-30 % |
+++ | +++ (++) | - | + (<20%) | 1 (2) |
Exzellent |
| Luminal B |
35-40 % |
++ | ++ (-) |
- | ++ (+++) |
2 (3) |
Intermediär |
| HER2-positiv | 15 % |
50 % pos. 50 % neg. |
+++ | Hoch | 2-3 | Schlecht | |
| Triple negativ |
15-20 % |
- | - | - | Hoch | 3 | Schlecht |
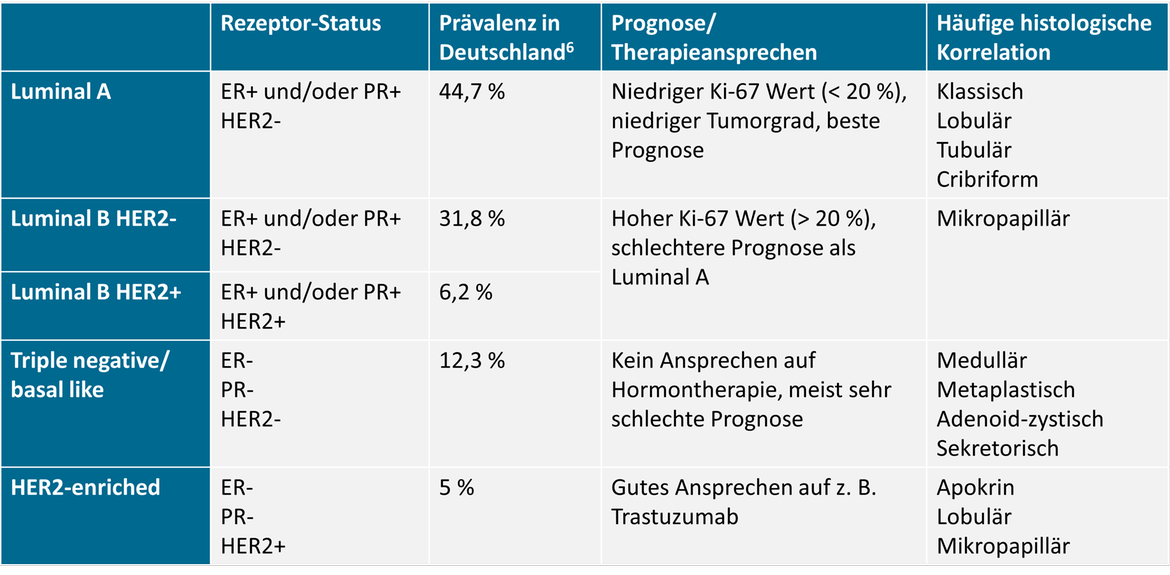
Die 5-Jahres-Überlebensrate der Patientinnen in den 5 Subtypen:
- Luminal A ist der prävalenteste Subtyp, weist aber die beste Prognose auf: 95,1 % (95 %-KI 93,7-96,5).
- Luminal B HER2+ hat eine etwas schlechtere Prognose mit 92,5 % (95 %-KI 87,9-97,1). Einen Hinweis auf den Verlauf gibt bereits der hohe Ki-67 Wert (> 20 %) bei diesen Patientinnen – er deutet auf ein schnelles Tumorwachstum hin.
- Luminal B HER2-: Mit 88,7 % (95 %-KI 86,2-91,2) weist dieser Subtyp eine schlechtere Prognose als Luminal B HER2+ auf.
- HER2-enriched: Mit 85,6 % (95 %-KI 78,6-92,6) liegt die Prognose bei diesem Subtyp etwas unter Luminal A bzw. B. Allerdings können diese Tumore mittlerweile gut therapiert werden mit Antikörpern gegen HER2-Rezeptoren.
- Triple-negativer Brustkrebs hat mit 78,5 % (95 %-KI 73,8-83,2) die schlechteste Prognose. Patientinnen mit Brustkrebs von diesem Subtyp sprechen nur auf Chemotherapie und nicht auf Hormontherapien an, weshalb sich eher ein schlechter Verlauf abzeichnet.
Die 5 Brustkrebstypen korrelieren zudem häufig mit einer speziellen histologischen Klassifikation. So weisen adenoid-zystische Tumore z. B. nur den molekularen Subtyp Triple-negative auf, während das tubuläre Mammakarzinom meist positiv für ER/PR und negativ für HER2 ist (Luminal A oder Luminal B HER2-).
Lobuläre Karzinome hingegen können sowohl den molekularen Subtyp HER2-enriched als auch den Typ Luminal A aufweisen. Auch mikropapilläre Tumore können unterschiedliche molekulare Subtypen sein: ER+ und/oder PR+ sowie HER2-/+ (Luminal B) und ER-/PR-/HER2+ (HER2-enriched).
| Stadium | Primärtumor | Lymphknotenstatus | Fernmetastasen |
| 0 | Tis | N0 | M0 |
| I | T1mic | N0 | M0 |
| T1a (1-5 mm) | N0 | M0 | |
| T1b (6-10 mm) | N0 | M0 | |
| T1c (11-20 mm) | N0 | M0 | |
| IIA | T0, T1mic, T1 | N1 | M0 |
| T2 (21-50 mm) | N0 | M0 | |
| IIB | T2 | N1 | M0 |
| T3 (>50 mm) | N0 | M0 | |
| IIIA | T0, T1mic, T1, T2 | N2 | M0 |
| T3 | N1 | M0 | |
| IIIB | T4* | N0-2 | M0 |
| IIIC | alle T | N3 | M0 |
| IV | alle T | alle N | M1 |
| *(Infiltration der Brustwand und/oder der Haut, und/oder ipsilaterale Satellitenmetastasen und/oder inflammatorisches Mammakarzinom) | |||
| N0 | keine befallenen Lymphknoten |
| N1 | 1-3 befallene Lymphknoten in der Axilla und/oder der ipsilateralen Mammaria-Interna-Region) |
| N2 | 4-9 befallene Lymphknoten |
| N3 | >9 befallene Lymphknoten |
Bei neu diagnostiziertem Brustkrebs ab dem UICC-Stadium II (UICC, Union Internationale Contre le Cancer) mit erhöhtem Risiko sowie Stadium III und IV ohne Symptomatik für eine Metastasierung sollte ein Staging (Lunge, Leber, Skelett) durchgeführt werden. Wegen höherer Sensitivität und Spezifität haben Computertomographie (CT) von Brustkorb/Bauch und Skelettszintigramm das frühere Staging mit Thorax-Röntgen und Bauch-Ultraschall ersetzt. Das Staging sollte nur durchgeführt werden bei Frauen mit höherem Metastasierungsrisiko (N+, > T2) und/oder aggressiver Tumorbiologie (zum Beispiel: HER2+, triple-negativ), klinischen Zeichen, Symptomen und bei geplanter Entscheidung zur systemischen Chemo-/Antikörpertherapie.
Chemotherapie:
Indikationen:
- bei HER2-positiven Tumoren ist eine simultane anti-HER2-gerichtete Antikörpertherapie in Kombination mit einer (neo-)adjuvanten Chemotherapie Standard
- bei endokrin nicht sensitiven Tumoren (ER- und PR-negativ)
- bei fraglich endokrin sensitiven Tumoren
- bei nodal-positiven Tumoren
- G3
- junges Erkrankungsalter (<35 Jahre)
Eine Chemotherapieindikation ergibt sich immer dann, wenn der individuelle zu erwartende Nutzen höher ist als mögliche Nebenwirkungen.
Bei Patientinnen mit einem primären Hormonrezeptor-positiven, HER2/neu negativen, nodal-negativen und nicht metastasierten Brustkrebs lassen die konventionellen Prognoseparameter einschließlich Ki-67 häufig keine eindeutige Entscheidung für oder gegen eine adjuvante Chemotherapie zu. Mit dem
Oncotype DX® Breast Recurrence Score Test steht ein prädiktiver Multigentest zur Verfügung, der eine individuelle Beurteilung des Rückfallrisikos und des zu erwartenden Nutzens einer adjuvanten Chemotherapie erlaubt. Der Test bestimmt die Ausprägung und Aktivität einer Gruppe von 21 Genen innerhalb eines Brustkrebsgewebes. Das Ergebnis der Analyse ist der Recurrence Score (RS), der in einem Bereich zwischen 0 und 100 liegt. Werte zwischen 0-25 werden so interpretiert, dass die Wahrscheinlichkeit für das Auftreten eines Fernrezidivs innerhalb von 9 Jahren gering ist und eine Chemotherapie dieses Rückfallrisiko nicht wesentlich senken würde. Ein höherer Wert identifiziert die Patientinnen, die von einer zusätzlich zur Hormontherapie durchgeführten Chemotherapie profitieren können.
Immuntherapie:
Anti-HER2-Therapie:
Etwa 20 % der invasiv-duktalen Mammakarzinome sind HER2/neu positiv, d. h. sie exprimieren vermehrt den HER2/neu-Rezeptor auf ihrer Zelloberfläche. Die Bindung eines sogenannten Liganden an diesen Rezeptor führt letzlich zu einer Zellproliferation, wehalb Patientinnen mit HER2/neu-positiven Tumoren häufig einen aggressiven Krankheitsverlauf mit einer frühen Metatasierung haben. Dagegen können zielgerichtete Substanzen zum Einsatz kommen, nämlich monoklonale Antikörper, die an unterschiedliche Epitope des HER2-Rezeptors binden und dadurch eine Zellproliferation unterbinden. Unter einer solchen Antikörpertherapie, beispielsweise mit
Trastuzumab (Herceptin®), können klinisch relevante
Herzinsuffizienzen auftreten. Deshalb ist ein Monitoring der linksventrikulären Herzauswurffraktion wichtig. EKG und Echokardiographie werden auch 6, 12, 24, 36, 48 und 60 Monate nach Abschluss der Therapie und danach alle 5 Jahre empfohlen.
Pertuzumab (Perjeta®) ist ein weiterer monoklonaler Antikörper, der in der Behandlung von HER2-positivem Brustkrebs eingesetzt wird. Patientinnen mit HER2-positivem Mammakarzinom und hohem Rezidivrisiko profitieren von einer Addition von Pertuzumab zur adjuvanten Therapie mit Trastuzumab und Chemotherapie. Der Einsatz zweier Antikörper wird als duale Blockade bezeichnet. Bei einer dualen Blockade ist die Wahrscheinlichkeit für das Auftreten von Diarrhoen (Durchfällen) erhöht.
CDK4/6-Hemmer:
Damit Ärzte einen CDK4/6-Inhibitor anwenden können, müssen die vorherigen Untersuchungen ergeben haben, dass der Brusttumor HER2-negativ und hormonrezeptorpositiv (ER+ und/oder PR+) ist.
Palbociclib, Ribociclib
und Abemaciclib können zum Einsatz kommen, wenn der Brustkrebs örtlich fortgeschritten oder metastasiert ist.
Abemaciblib und Ribociclib sind auch für Frauen mit frühem Brustkrebs ergänzend (adjuvant) zugelassen, wenn sie ein hohes Rückfallrisiko haben.
CDK4/6-Hemmer sind Medikamente zum Schlucken – entweder in Kapsel- oder Tablettenform. Frauen erhalten sie in Kombination mit einer Antihormontherapie.
Neben- und Folgewirkungen sowie Langzeitkomplikationen der Chemo- und Strahlentherapien:
Typisch postoperative Komplikationen sind die Serombildung im OP-Gebiet, Wundinfektionen, Sensibilitätsstörungen, Schmerzen an der Brustwand bzw. in der Brust bei Brusterhaltender Therapie, Bewegungseinschränkungen und das
Armlymphödem .
Bei Chemo-, Strahlen-, Antikörper- und Hormontherapien kann es ebenfalls zu typischen Nebenwirkungen kommen. Zu den häufigsten Folgen zählen Osteoporose, Kardiotoxizität (Schädigung des Herzens) und Thromboembolien. Eine frühzeitige therapieinduzierte Menopause erhöht das Risiko einer Osteoporose sowie pathologischen Fraktur. Fatigue, ein chronisches Erschöpfungs- und Müdigkeitssyndrom, kann nach jeder Behandlung eines Mammakarzinoms auftreten. Wichtigste naturheilkundliche therapeutische Maßnahme einer
Fatigue ist die Bewegungstherapie. Ernährungstherapeutisch sind eine Steigerung der Flüssigkeitsmenge auf mindestens 2 Liter täglich sowie wenig fett- und zuckerhaltige Speisen zu empfehlen. Unter Chemotherapien kommt es zu einem vermehrten Verlust von L-Carnitin, welches am Energieumsatz der Muskelzellen beteiligt ist. Eine Substitution führt zur Leistungssteigerung und damit zu Verbesserung der Fatigue-Symptomatik. Als Dosierung werden 1-4 g täglich für 4-6 Wochen empfohlen.
Chemotherapie:
Übelkeit, Erbrechen, Neutropenie (Verminderung bestimmter weißer Blutkörperchen) und Haarausfall sind regelmäßige Nebenwirkungen der Chemotherapien. Auch Anämien kommen häufig vor. Leichte
Entzündungen der Mundschleimhaut können durch
Salbei anwendungen in Form eines Tees oder das Präparat Salviathymol® N gelindert werden. Auch das Lutschen kleiner Eisstücke oder die Anwendung lokaler Anästhetika kann helfen. In schweren Fällen stehen sogenannte Mucositis-Lösungen zur Verfügung. Gegen das
Hand-Fuß-Syndrom werden 10 %
harnstoffhaltige Salben engesetzt. Einige Chemotherapeutika, die
Anthrazykline,
können das Herz schädigen oder in seltenen Fällen eine akute myeloische
Leukämie induzieren. EKG und Echokardiographie werden 6, 12, 24, 36, 48 und 60 Monate nach Therapieende mit Anthrazyklinen und danach alle 5 Jahre empfohlen.
Strahlentherapie:
Zu den kurzfristigen Begleiterscheinungen zählen
- die radiogene Hyperthermie (Überwärmung)
- das radiogene Erythem (Hautrötung)
- das radiogene Hautödem
- die Hyperpigmentierung
- trockene und feuchte Epitheliolysen (Hautabhebungen)
Die Hautreaktionen verlaufen verzögert. Sie beginnen meistens 2-3 Wochen nach der ersten Bestrahlung und werden dann im Lauf der Behandlung allmählich stärker. Der Höhepunkt wird gegen Ende der Bestrahlung oder in der ersten Woche nach der Strahlentherapie erreicht. Danach klingen die Hautreaktionen wieder ab. Drei bis vier Wochen nach Ende der Strahlentherapie ist die Hautreaktion auch bei schwerem Verlauf fast immer vollständig abgeklungen. Der Verlauf der Hautreaktionen hängt von vielen individuellen Faktoren ab. Bestimmte Medikamente (vor allem Chemotherapeutika) oder Rauchen können zu stärkerer Hautreaktion beitragen.
Beachten Sie bitte folgende Verhaltensregeln:
- Die bestrahlte Haut neigt zu Allergien. Vermeiden Sie deshalb parfümierte Seifen oder Deos; diese enthalten nämlich viele chemische Zusätze und lösen besonders leicht Allergien aus. Am besten verwenden Sie klares Wasser oder eine medizinische Seife (z. B. Dermowas®).
- Zur Hautpflege wird häufig ein Babypuder empfohlen. Puder vergrößert die Hautoberfläche. Somit kann die Wärme in der Haut besser abstrahlen, zudem halten Feldmarkierungen, die für die Bestrahlung nötig sind, auf der trockenen Haut besser. Bei leichter Hautrötung behalten Sie die Pflege mit Puder bei. Sie können aber auch mit ureahaltigen Lotionen, Linola® Radio-Derm, Bepanthen Lotion oder Aloe Vera Gel pflegen – all diese Substanzen wirken entzündungshemmend. Eine solche Hautpflege wird von vielen Patientinnen als angenehm empfunden, weil die Haut dann nicht so sehr spannt. Prüfen Sie, ob dies auch bei Ihnen hilft. Kühlen Sie eventuell das Bestrahlungsfeld mit Kühlgelkissen.
- Vermeiden Sie wegen der Empfindlichkeit der Haut scheuernde oder enge Kleidungstücke, zu heißes oder zu kaltes Wasser.
- Frische Luft und Sonne sind erlaubt. Vermeiden Sie aber starke Sonneneinstrahlung auf die Haut im Bestrahlungsfeld oder gar einen Sonnenbrand; dieser würde in der bestrahlten Haut sehr viel heftiger verlaufen.
Alle Verhaltensregeln gelten natürlich nur für die bestrahlte Haut. Außerhalb der Bestrahlungsfelder gibt es keine Einschränkungen.
Zu den möglichen langfristigen Folgeerscheinungen zählen:
- die strahleninduzierte Fibrose und Anisomastie (Asymmetrie der Brüste)
- Radioderm (fleckförmige Pigmentanomalien, Teleangiektasien und straffe Hautatrophie (bis zur Geschwürsbildung = chronisches Strahlenulkus)
- die Hyperästhesie
- das chronische Hautödem
- das Erysipel und der Herpes zoster
- das strahleninduzierte Sarkom
Adjuvante Hormontherapie:
Patientinnen mit Estrogen- und/oder Progesteron-positiven invasiven Tumoren sollen unabhängig von einer möglichen Chemotherapie eine endokrine Therapie erhalten. Diese soll erst nach Abschluss der Chemotherapie begonnen werden, kann aber parallel zur Strahlentherapie erfolgen. Als endokrin sensitiv gelten die Tumoren mit mindestens 10 % Hormonrezeptor-positiver Zellen, wobei hier der Estrogenrezeptor die entscheidende Rolle zu spielen scheint. Bei 1-10 % positiver Zellen spricht man von einer fraglichen endokrinen Sensitivität, bei <1 % vom Hormonrezeptor-negativen Brustkrebs.
Adjuvante endokrine Therapien reduzieren auch in Langzeitdaten signifikant die Wahrscheinlichkeit eines Rezidivs. So führt die Einnahme von Tamoxifen über fünf Jahre bei Patientinnen mit ER-positivem Mammakarzinom zu einer absoluten Risikoreduktion für ein Rezidiv von 4,8 % auf 2,9 %.
Die vorteilhaften Effekte der endokrinen Therapie werden nur bei ausreichender Therapieadhärenz realisiert. Aber nur etwa die Hälfte der Frauen mit Brustkrebs führen diese Behandlung über die empfohlenen fünf Jahre durch. Dieser Mangel an Compliance ist mit einer signifikant erhöhten brustkrebsspezifischen Mortalität verbunden (absolute Risikoreduktion der brustkrebsspezifischen Mortalität von 27,1 % auf 19,3 % durch die Einnahme von Tamoxifen über einen Zeitraum von fünf Jahren). Bei schweren Nebenwirkungen, welche die Therapieadhärenz reduzieren, kann bei postmenopausalen Patientinnen der Wechsel von einem Aromatasehemmer auf Tamoxifen und umgekehrt oder zwischen den Aromatasehemmern (steroidal, also Exemestan vs. nicht steroidal, also Anastrozol oder Letrozol) erwogen werden.
Bei prämenopausalen Patientinnen soll eine Tamoxifentherapie (20 mg tgl.) für mindestens fünf Jahre durchgeführt werden. In Abhängigkeit des Rezidivrisikos soll eine Einnahme über zehn Jahre nach Erstdiagnose beziehungsweise bis zum Rezidiv erwogen werden. Die Ovarialsuppression (GnRH-Analoga oder bilaterale Ovarektomie) zusätzlich zu Tamoxifen oder einem Aromatasehemmer soll nur bei hohem Rezidivrisiko und prämenopausaler Situation nach adjuvanter Chemotherapie erwogen werden. Die adjuvante endokrine Therapie für postmenopausale Patientinnen mit einem ER-positiven Mammakarzinom sollte einen Aromatasehemmer enthalten.
Grundlegende Prinzipien der adjuvanten endokrinen Therapie:
- 5 Jahre endokrine Therapie sind der Standard
- Eine erweiterte adjuvante Therapie über 5 Jahre hinaus sollte nur bei hohem Rückfallrisiko erwogen werden
- Es existiert kein valider Biomarker bzw. Prädiktor für oder gegen eine erweiterte adjuvante Therapie
- Art und Dauer der Therapie sollten sich an der Histopathologie, dem Menopausenstatus, der Verträglichkeit und dem Rezidivrisiko orientieren
- Der Wechsel auf eine andere endokrine Therapie (Tamoxifen oder Aromatasehemmer oder umgekehrt) ist besser als die Therapie zu stoppen
- Beginn mit Aromatasehemmer bei höherem Rückfallrisiko (N+) oder/und lobulärem Karzinom
- Tamoxifen ist bei geringerem Risiko, höherem Alter und Komorbidität eine adäquate Therapie
Risikofaktoren, die eine erweiterte endokrine Therapie für mehr als 5 Jahre begründen können:
- Alleinige Tamoxifen-Therapie (wenn Patientin zum Zeitpunkt der Entscheidungsfindung postmenopausal)
- Zustand nach Chemotherapie (da Patientinnen in der Regel high-risk)
- T2 - T4-Tumoren
- Nodalpositiv (Lymphknotenbefall)
- Hohes Rückfallrisiko basierend auf immunhistochemischen Markern oder Genexpressionsprofilen zum Zeitpunkt der Erstdiagnose
- Erhöhter CTS5-Score (siehe unten)
Antiöstrogen Tamoxifen:
Tamoxifen blockiert den Östrogen-Rezeptor in den Krebszellen. Die Standarddosierung beträgt 20 mg täglich.
Die Patientinnen klagen häufig über
Hitzewallungen . Dagegen wird heute vor allem der Einsatz von Psychopharmaka empfohlen. Einige Psychopharmaka, sogenannte SSRI (Selektive Serotonin-Wiederaufnahmehemmer), wie Paroxetin oder Fluoxetin hemmen jedoch die Funktion des Leberenzyms Cytochrom P 450 2 D6, welches Tamoxifen erst in seine wirksame Form überführt. Dies kann die Tamoxifen-Plasmakonzentration um 65-75 % senken. Die Hitzewallungen unter Einnahme von Tamoxifen können stattdessen versuchsweise mit dem Antidepressivum
Venlafaxin (eine Woche lang 37,5 mg tgl., danach 75 mg tgl.; typische Nebenwirkungen Mundtrockenheit, Übelkeit, Appetitlosigkeit) behandelt werden, einem sogenannten SNRI (Serotonin-Noradrenalin-Wiederaufnahmehemmer). Auch das Antidepressivum Citalopram kann in einer Tagesdosis von 20 mg Citalopram wirken, hemmt aber ebenfalls leicht das Leberenzym Cytochrom P 450 2 D6. Unter Psychopharmaka-Einnahme werden regelmäßige Laborkontrollen (z. B. Blutbild, Natrium, Kalium, GOT, GPT, GGT; Bilirubin, CK, Glukose) empfohlen.
Alternativ können das Antikonvulsivum Gabapentin (3x 300 mg tgl.; einschleichende Einnahme; Nebenwirkungen Ödeme, Schwindel, Verwirrtheit) oder ein Behandlungsversuch mit dem Anticholinergikum Methantheliniumbromid (Vagantin®, 3x tgl. eine Tablette 15-30 Minuten vor den Mahlzeiten) erfolgen. Dessen stärkste Nebenwirkung stellt eine ausgeprägte Mundtrockenheit dar. Auch Oxybutynin, ein Anticholinergikum, das eingesetzt wird bei Harninkontinenz und überaktiver Blase, kann Hitzewallungen unterdrücken. Die genannten Alternativen werden praktisch kaum eingesetzt.
Unter dem Antiöstrogen steigt das
Thromboserisiko um das Dreifache. Dieser Östrogenantagonist ist bei Hinweisen auf Thromboserisiken kontraindiziert.
Zyklusstörungen, vaginale Trockenheit und Stimmungsschwankungen treten genauso häufiger auf wie Muskel- und Gelenkschmerzen.
Der Augenhintergrund sollte unter Einnahme von Tamoxifen einmal im Jahr kontrolliert werden wegen der möglichen Gefahr der Entwicklung eines
Katarakts (Trübung der Augenlinse) oder von
Netzhautveränderungen .
Nach mehrjähriger Einnahme ist das Risiko für ein
Endometriumkarzinom etwas erhöht. Nach 1- bis 2-jähriger Einnahme verdoppelt sich das relative Risiko für die Entwicklung eines Endometriumkarzinoms, bei mindestens 5-jähriger Einnahme vervierfacht sich das Risiko. Trotzdem empfiehlt die Leitlinie Endometriumkarzinom keine routinemäßge Transvaginalsonographie.
Unter Tamoxifen wird häufiger auch eine Abnahme des sexuellen Interesses beobachtet, eine wirksame Behandlung dafür gibt es nicht.
Aromatasehemmer (Anastrozol, Letrozol, Exemestan):
Aromatasehemmer unterbinden die Östogenproduktion im Muskel- und Fettgewebe durch Blockade des Enzyms Aromatase. Die nichtsteroidalen Aromatasehemmer Letrozol und Anastrozol erreichen dies durch eine kompetitive Bindung am Hämanteil der Aromatase, der steroidale Aromatasehemmer Exemestan durch eine irreversible Inaktivierung der Aromatase. Ein Ansatz in der Prämenopause kann über eine Aktivierung der Gonadotropin-Achse zu einer unerwünschten ovariellen Stimulation führen, weshalb sie nur postmenopausal eingesetzt werden können. Ein Aromatasehemmer für 2-3 Jahre gilt als fester Bestandteil der initialen endokrinen Therapie in der Postmenopause, während die 5-jährige Aromatasehemmer-Therapie bei lobulären Karzinom sowie bei erhöhtem Rückfallrisiko empfohlen wird. Während die Effektivität aller 3 Aromatasehemmer grundsätzlich als äquivalent gilt, scheinen die nichtsteroidalen Aromatasehemmer bei Patientinnen mit invasiv lobulärem Karzinom Exemestan überlegen zu sein. Eine mehrjährige Medikation führt zu einem höheren Knochendichteverlust und einer höheren Rate osteoporotischer Frakturen. Der Fachbegriff lautet Tumortherapie-induzierte Osteoporose. Deshalb sollte vor Beginn einer Aromatasehemmer-Medikation eine Knochendichtemessung erfolgen.
Nebenwirkungsprofile von Aromatasehemmern und Tamoxifen im Vergleich:
| Nebenwirkung | Aromatasehemmer | Tamoxifen |
|---|---|---|
| Arthralgie/Myalgie | +++ | + |
| Osteoporose | ++ | |
| Wechseljahrsbeschwerden | + | +++ |
| Endometriumkarzinom | + | |
Thromboembolische Komplikationen |
++ | |
| Sehstörungen | + | |
| Hypercholesterinämie | + |
In Anlehnung an die Leitlinien des Dachverbandes Osteologie wird in Deutschland das nachfolgende Schema zur Beurteilung der Behandlungsbedürftigkeit einer Osteoporose verwendet:
Eine Alternative zur Berechnung des Frakturrisikos ist das weltweit bevorzugte computergestützte Programm FRAX (Fracture Risk Assessment Tool).
Beide Kalkulatoren berechnen die Therapieschwelle zur Intervention für ein Frakturrisiko von 20% über 10 Jahre.
Eine Substitution mit
Kalzium (1000-1500 mg/Tag) und/oder
Vitamin D (800-2000 I.E./Tag) wird fast immer empfohlen. Die Bestimmung des
Vitamin-D-Spiegels kann zu Beginn der Therapie und zu einer einmaligen späteren Kontrolle sinnvoll sein. Zusätzlich sind
Biphosphonate bei nachgewiesener Osteopenie oder manifester Osteoporose indiziert (T-score <-1,5 SD bei einem weiteren Fraktur-Risikofaktor bzw. T-score <-2,0; Achtung: selten Gefahr von
Kieferosteonekrosen, siehe unten). Häufig erfolgt solch eine Frakturprävention mit 4 mg Zoledronat intravenös alle 6 Monate über 3 Jahre hinweg. Wichtig sind Nikotinverzicht, nur mäßiger Alkoholkonsum und die Vermeidung von Untergewicht (BMI <20 kg/m²). Wenn die Knochendichtemessung zu Beginn einer antihormonellen Behandlung normal ausfällt, kann eine zweite Messung nach 2-3 Jahren erfolgen.
Weitere häufige Nebenwirkungen unter Aromatasehemmern sind
Gelenk-, Knochen- und Muskelschmerzen. Die Häufigkeiten werden wie folgt angegeben: Anastrozol 35,6 %, Letrozol 28,5 %, Exemestan 18 %. Die wichtigste Maßnahme zur Linderung ist gelenkschonende Ausdauerbewegung, z. B. 5x wöchentlich für 30 Minuten. Naturheilkundlich ist eine Medikation mit antiphlogistischer und analgetischer Wirkung möglich, wie sie bei der naturheilkundlichen Rheumatologie ihre Anwendung findet. Substanzen wie Teufelskralle (z. B. Teltonal® 2x1 Tablette täglich), Brennesselextrakt (z. B. Rheuma Hek® 2x2 Tabletten täglich) oder Weidenrindenextrakt (z. B. Assalix® 1-2x 1 Dragee täglich) können dafür angewendet werden. Eine medikamentöse Schmerztherapie kann mit einem traditionellen nicht steroidalen Antirheumatikum (tNSAR) wie Ibuprofen oder einem Cyclooxygenasehemmer-2-selektiven NSAR wie Arcoxia® oder Celebrex® erfolgen. Letztere gelten bei Patientinnen mit Risiken für Magen-Darm-Erkrankungen anstelle der tNSAR als erste Wahl. Wenn sie kontraindiziert sind (z. B. bei Niereninsuffizienz, Herzinsuffizienz NYHA II-IV, schwerer Leberfunktionsstörung, schlecht eingestelltem Bluthochdruck, koronarer Herzkrankheit, Zustand nach Schlaganfall) können tNSAR bei Patientinnen mit Risiken für Magen-Darm-Erkrankungen mit Protonenpumpenhemmern kombiniert werden. Bestehen Kontraindikationen gegen NSAR oder sind beide Substanzen nicht wirksam, kann eine Kombinationstherapie eines NSAR mit einem schwachen Opioid wie Tilidin oder Tramadol versucht werden. Auch die pflanzlichen Enzyme Papain und Bromelain sowie Selen und Lektin können eine alternative Behandlungsmöglichkeit darstellen (z. B. in Form von 2 Tbl. Sanomucin® tgl. morgens vor dem Frühstück).
Auch
Scheidentrockenheit und Schmerzen bei Geschlechtsverkehr können verstärkt auftreten. Vaginale Gleitmittel und Feuchtigkeitscremes lindern diese Beschwerden.
Eine erweiterte adjuvante Therapie über insgesamt 6-10 Jahre bringt für nodal-positive Patientinnen einen Vorteil im Gesamtüberleben. Die Patientinnen unter erweiterter adjuvanter Therapie müssen über die Zunahme der Nebenwirkungen aufgeklärt werden. 10 versus 5 Jahre Tamoxifen-Therapie verdoppeln die Rate der Endometriumkarzinome, eine verlängerte Aromatasehemmer-Einnahme ist mit signifikant höheren Osteoporoseraten sowie deutlich erhöhten Frakturraten verbunden.
Osteoonkologische Therapie mit Biphosphonaten:
Biphosphonate wie Zoledronsäure werden häufig zur Prävention und Therapie einer therapieassoziierten Osteoporose intravenös verabreicht, gelegentlich auch zur Therapie von Knochenmetastasen. In ca. 1 % der Fälle kommt es dabei zur Ausbildung von
Kieferosteonekrosen. Diese sind definiert als Wunden mit freiliegendem Knochen im Ober- oder Unterkiefer, die trotz adäquater Behandlung über mindestens acht Wochen keine Tendenz zur Sekundärheilung zeigen. Sie gehen dabei häufig mit einer Entzündung der Mundschleimhaut und Abszessbildung einher. Risikofaktoren stellen Infektionen im Knochen dar, wie sie beispielsweise im Zusammenhang mit Zahnextraktionen, Implantaten, Wurzelspitzenresektionen, Parodontalchirurgie, Prothesen (Druckstellen), Parodontalerkrankungen sowie einer generell schlechten Mundhygiene entstehen. Weitere Risikofaktoren sind unter anderem Alkohol- und Nikotinkonsum, Diabetes mellitus, Adipositas und Niereninsuffizienz. Eine Zahnsanierung sollte vor Beginn einer Biphosphonattherapie erfolgen, zahnärztliche Kontrollen im Abstand von 6 Monaten. Elektive invasive Zahneingriffe sollten vermieden werden. Falls invasive Eingriffe im Mundkieferbereich notwendig sind, sollten diese im Idealfall mindestens sechs bis acht Wochen vor Beginn der Therapie terminiert werden und komplett ausgeheilt sein. Sollte eine Wurzelbehandlung unter Therapie nötig sein, ist eine systemische, perioperative antibiotische Prophylaxe vorzunehmen.
Nachsorge von Brustkrebs:
Die Nachsorge bei Patientinnen mit Mammakarzinom beginnt mit der abgeschlossenen lokoregionären Primärbehandlung. Sie besteht aus Anamnese, körperlicher Untersuchung, ärztlicher Beratung, Betreuung und Begleitung sowie bildgebender Diagnostik zur Erkennung eines lokal- und lokoregionären Rezidivs und eines kontralateralen Mammakarzinoms. Die Kontrolluntersuchungen sollten in den ersten 3 Jahren vierteljährlich, in den Jahren 4 und 5 halbjährlich und ab dem 6. Jahr jährlich erfolgen. Die üblichen jährlichen Untersuchungen zur Krebsfrüherkennung sind in die Nachsorge einzubetten.
Bei nach Primärtherapie asymptomatischen Patientinnen ist die Nachsorge konservativ auszurichten; sie umfasst die Selbstuntersuchung der Brust durch die Patientin, die Untersuchungen beim Frauenarzt, die Mammographie, die Mammasonographie und in Einzelfällen die
Kernspinuntersuchung (MRT) der Brustdrüse. Eine weitergehende apparative (Skelettszintigraphie, Röntgen-Thorax, Lebersonographie) oder serologische Nachsorge (Blutabnahme) wird von den Fachgesellschaften nicht befürwortet.
Im engeren Sinne dient die Tumornachsorge der Früherkennung lokaler sowie sogenannter lokoregionärer Rezidive sowie eines Mammakarzinoms auf der Gegenseite. Gleichrangig sind klinische Hinweise auf Fernmetastasen und nicht zuletzt unerwünschte Nebenwirkungen einer noch laufenden Therapie zu berücksichtigen. Im Gegensatz zu vielen anderen bösartigen Tumoren besteht die Primärtherapie beim Mammakarzinom nicht nur aus der Operation, sondern vielleicht noch aus einer Bestrahlung und/oder medikamentösen Therapien in Form von einer Chemotherapie, einer Antikörpertherapie, auch Immuntherapie genannt, oder einer Hormontherapie. Letztere kann sich im Extremfall über mehr als 5 Jahre erstrecken. In diesen Fällen muss man sich von der üblichen Nachsorgedefinition (Beginn erst nach vollständigem Abschluss der Primärtherapie) lösen und die Nachsorge schon nach der Primäroperation, also bereits parallel zu einer noch laufenden Primärtherapie starten. Grundsätzlich ist die körperliche sowie psychische und soziale Rehabilitation gleichrangig anzugehen.
Die Patientinnen gelten, sofern keine verdächtigen Symptome bestehen, welche auf einen Rückfall hinweisen, oder schon Metastasen gesichert sind, als tumorfrei. Mögliche Frühsymptome eines Rückfalls sind:
- Auffälliger Tastbefund an der Brust
- Knochenschmerzen
- Atemnot
- Bauchschmerzen
- Kopfschmerzen
Frauen mit hohem familiären Risiko sollten über die Möglichkeit einer genetischen Beratung aufgeklärt werden.
Bei Frauen nach einer Brust erhaltenden Therapie steht eine erste Nachsorge-Mammographie frühestens 6 Monate nach Abschluss der lokalen Primärtherapie an.
Rezidive manifestieren sich klinisch als Lokalrezidiv an der betroffenen Brust oder nach Brustamputation an der Wand des Brustkorbs und der darüber liegenden Haut oder als lokoregionäre Rezidive in den Lymphknoten der Achselhöhle, oberhalb oder unterhalb des Schlüsselbeins oder entlang der sogenannten Mammaria-interna-Gefäße. Bevorzugte Lokalisationen von Fernmetastasen sind das Skelettsystem, die Lunge, das Rippenfell und die Leber.
| Nachsorge/Follow-Up*: | Screening: | |||
| Jahre nach Primärtherapie | 1. 2. 3. | 4. 5. | >5 | |
| Anamnese, klinische Untersuchung, Beratung | invasiv: alle 3 Monate | invasiv: alle 6 Monate | invasiv: alle 12 Monate | |
| CLIS/DCIS: alle 6-12 Monate | CLIS/DCIS: alle 12 Monate | |||
| Selbstuntersuchung | monatlich | |||
| Bildgebende Diagnostik, Laboruntersuchungen | indiziert nur bei Symptomatik +/- Befunden
+/- Verdacht auf Rezidiv/Metastasen |
|||
| Mammographie und Sonographie | invasiv: BET** | beidseits: alle 12 Monate | ||
| invasiv: Mastektomie | kontralateral: alle 12 Monate | |||
| CLIS/DCIS | alle 12 Monate | |||
| *Fortlaufende Nachsorgeuntersuchungen bei noch laufender adjuvanter Therapie
**Erste Mammographie nach BET 6-12 Monate nach komplettierter Radiatio |
||||
Bei niedrigem Rezidivrisiko kann nach 10 Jahren Nachsorge die Frequenz der Mammographie auf alle 2 Jahre ausgedehnt werden. Bei normalem sowie höherem Rezidivrisiko wird die Nachsorge in jährlichen Abständen fortgeführt.
Digitale Gesundheitsanwendungen (DiGA):
Mit dem Digitale-Versorgung-Gesetz (DVG) ist neben dem Anspruch der Versicherten auf Leistungen wie Hilfsmittel ein neuer Leistungsanspruch auf Versorgung mit DiGA eingeführt worden. .
DiGA sind digitale Medizinprodukte, die die Versicherten etwa bei der Behandlung von Erkrankungen oder dem Ausgleich von Beeinträchtigungen unterstützen können. Eine häufige Form sind Gesundheits-Apps für das Smartphone, aber es gibt auch browserbasierte Webanwendungen oder Software zur Verwendung auf klassischen Desktop-Rechnern.
Die DiGA optimune behandelt die Schwerpunktthemen Ernährung, Bewegung, Sport, Psyche sowie Schlaf.
Die DiGA PINK! bietet fachlich kompetente, gut verständliche und umfassende Informationen - empathisch aufbereitet, wissenschaftlich fundiert und leitlinienkonform. In Form von Videos, Podcasts und Texten finden Sie hier vielfältige Informationen zu Diagnose, Therapie, Nachsorge und zahlreichen organisatorischen Fragen.
Zusätzlich bietet PINK! noch kostenlose interaktive Formate wie die telefonische Sprechstunde oder die Webinar-Reihe "Frag doch mal PINK!" mit Fachexperten an.
Gesundheits-App:
Sidekick Health ist eine interaktive kostenlose Gesundheits-App mit einem 14-wöchigen Brustkrebs-Programm, das vor allem in der herausfordernden Zeit der Behandlung unterstützend zur Seite steht und den Weg ein wenig erleichtern möchte.
Auf folgende Weise unterstützt das Programm über 14 Wochen:
- Erfahre mehr über Diagnose, Behandlung und potenzielle Nebenwirkungen und lerne, leichter damit umzugehen.
- Erhalte Zugriff auf Techniken, mit denen man Stress erkennt und reduziert.
- Baue gesunde Gewohnheiten für besseren Schlaf auf.
- Lerne, wie Bewegung dein Wohlbefinden während der Krebsbehandlung positiv beeinflussen kann.
- Ernähre dich gesund - während deiner Behandlung und darüber hinaus.
- Übe dich in Achtsamkeit und Selbstmitgefühl in dieser herausfordernden Zeit.
- Lass dich automatisch daran erinnern ausreichend Wasser zu trinken oder deine Medikamente zu nehmen.
Brustkrebs beim Mann:
Ca. 1 % aller Mammakarzinome treten bei Männern auf. Es gibt etwa 700-800 Neuerkrankungen im Jahr. Das mittlere Erkrankungalter liegt bei 71 Jahren.
Ursachen:
- Imbalance des Östrogen/Testosteron-Gleichgewichts
- Regionale Häufung (Nord- und Westafrika)
- Familiäres Risiko
- Exogene Hormonzufuhr
- Stoffwechselstörungen, z. B. Leberzirrhose
- Strahlenexposition der Brustwand
- Transgender
- Adipositas, Gynäkomastie
Genetische Faktoren:
- bis zu 20 % haben Verwandte 1. Grades mit Mammakarzinom
- bis zu 40 % sind BRCA2-Mutationsträger (< 5 % BRCA1), BRCA2-Mutation 80fach ↑ Erkrankungsrisiko
- ca. 5 % zeigen Karyotyp XXY (Klinefelter-Syndrom), 20−60fach ↑ Erkrankungsrisiko
Klinisches Bild:
- 70−90 % schmerzloser Knoten im retromamillärem Brustsegment
- 20 % Veränderung der Mamille
- Metastasen-abhängige Symptome
- 40 % ED im fortgeschrittenem Tumorstadium (≥ IIb)
Diagnostik:
- Klinisch
- Bildgebende Kombination: Mammographie und Sonographie
- Histologische Abklärung per Stanze/Punchbiopsie
- Ggf. MRT zur Abklärung der Thoraxwand
- Umfelddiagnostik, da deutlich erhöhte Rate an Zweitmalignomen (v. a. Prostata)

